Notícia
FDA permite a comercialização do primeiro dispositivo médico para alívio da dor associada à síndrome do intestino irritável
Dispositivo foi aprovado (para comercialização nos Estados Unidos) para auxiliar na redução da dor abdominal funcional em pacientes de 11 a 18 anos de idade com síndrome do intestino irritável, quando combinado com outras terapias
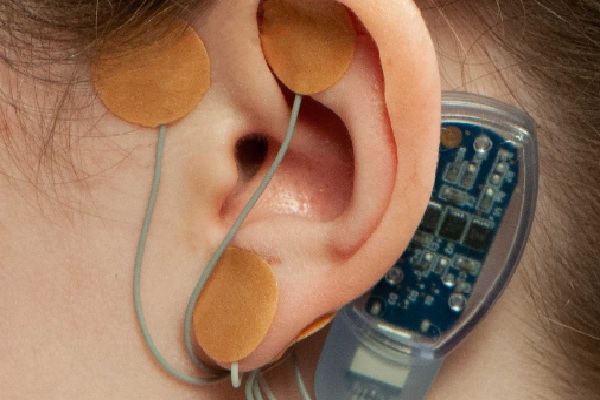
Divulgação, Innovative Health Solutions
Fonte
FDA | U.S. Food and Drug Administration
Data
sábado, 8 junho 2019 14:40
Áreas
Bioeletrônica. Medicina. Neurociências. Regulação.
A agência reguladora dos Estados Unidos FDA (U.S. Food and Drug Administration) autorizou no último dia 7 de junho a comercialização (nos Estados Unidos) do primeiro dispositivo médico para auxiliar na redução da dor abdominal funcional em pacientes de 11 a 18 anos de idade com síndrome do intestino irritável (SII) quando combinada com outras terapias para a SII. A SII é uma condição que afeta o intestino grosso que pode causar dor abdominal e desconforto tipicamente relacionados aos movimentos intestinais.
“Este dispositivo oferece uma opção segura para o tratamento de adolescentes com dor de SII através do uso de estimulação nervosa leve”, disse o Dr. Carlos Peña, diretor do Escritório de Dispositivos de Medicina Física e Neurológica do Centro de Dispositivos e Saúde Radiológica da FDA. “A ação reflete nosso compromisso contínuo com o avanço do desenvolvimento de dispositivos médicos pediátricos para que crianças e adolescentes tenham acesso a dispositivos médicos seguros e eficazes que atendam às suas necessidades.”
O IB-Stim é um dispositivo que necessita de prescrição médica composto de um pequeno estimulador elétrico de uso único que é colocado atrás da orelha do paciente. Ele contém um chip alimentado por bateria que emite pulsos elétricos de baixa freqüência para estimular ramos de certos nervos cranianos continuamente por cinco dias, quando então é substituído. Estimular feixes nervosos dentro e ao redor da orelha pode ser uma solução para o alívio da dor. Os pacientes podem usar o dispositivo por até três semanas consecutivas para reduzir a dor abdominal funcional associada à SII.
A FDA revisou dados de um estudo clínico publicado que incluiu 50 pacientes de 11 a 18 anos de idade com SII – 27 pacientes foram tratados com o dispositivo e 23 pacientes receberam um dispositivo placebo. O estudo mediu a mudança da linha de base até o final da terceira semana em pior dor abdominal, dor habitual e escores de duração da gravidade da dor (PFSD), que incorporam múltiplos aspectos da experiência da dor. Alterações nas evacuações não foram avaliadas. Durante o estudo, os pacientes foram autorizados a continuar doses estáveis de medicação para tratar a dor abdominal crônica. A pior dor no início do estudo foi semelhante entre os grupos de tratamento e placebo. Uma análise de medidas repetidas mostrou melhora na dor desde o início até a terceira semana no grupo de tratamento. Este efeito também foi observado nas semanas um e dois. Maior mudança também foi demonstrada em pontuações PFSD composta desde o início até a terceira semana no grupo IB-Stim comparado ao grupo placebo. O tratamento com IB-Stim resultou em pelo menos 30% de redução da dor habitual ao final de três semanas em 52% dos pacientes tratados, em comparação com 30% dos pacientes que receberam placebo Durante o estudo, seis pacientes relataram desconforto leve no ouvido e três pacientes relataram alergia ao adesivo no local de aplicação.
O dispositivo foi contraindicado para pacientes com hemofilia, pacientes com marca-passos cardíacos ou aqueles diagnosticados com psoríase vulgar (uma condição na qual as células da pele se acumulam e formam escamas e placas secas).
Acesse a notícia completa na página da FDA (em inglês).
Fonte: Sandy Walsh, FDA. Imagem: Divulgação, Innovative Health Solutions.
Em suas publicações, o Portal Tech4Health da Rede T4H tem o único objetivo de divulgação científica, tecnológica ou de informações comerciais para disseminar conhecimento. Nenhuma publicação do Portal Tech4Health tem o objetivo de aconselhamento, diagnóstico, tratamento médico ou de substituição de qualquer profissional da área da saúde. Consulte sempre um profissional de saúde qualificado para a devida orientação, medicação ou tratamento, que seja compatível com suas necessidades específicas.
Os comentários constituem um espaço importante para a livre manifestação dos usuários, desde que cadastrados no Portal Tech4Health e que respeitem os Termos e Condições de Uso. Portanto, cada comentário é de responsabilidade exclusiva do usuário que o assina, não representando a opinião do Portal Tech4Health, que pode retirar, sem prévio aviso, comentários postados que não estejam de acordo com estas regras.




Apenas usuários cadastrados no Portal tech4health t4h podem comentar, Cadastre-se! Por favor, faça Login para comentar